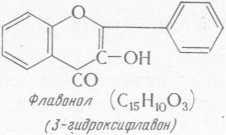
жиры лучше всего растворяются в
Жиры лучше всего растворяются в
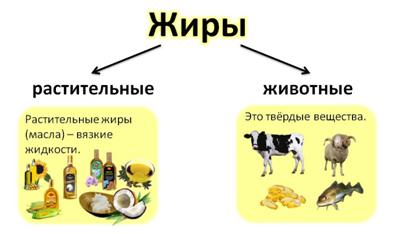
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров есть некоторые важные отличия.
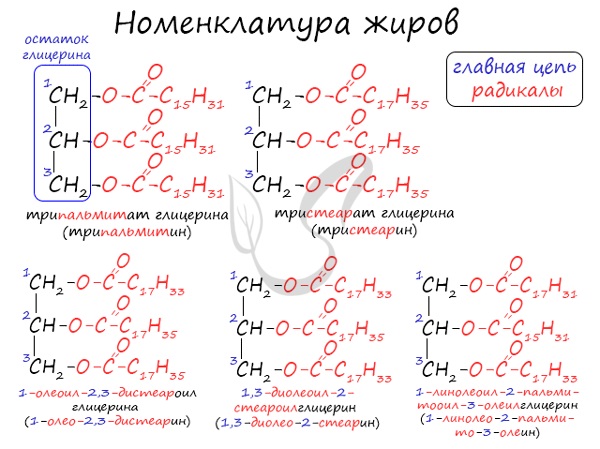
Номенклатура жиров
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать 😉
Получение жиров
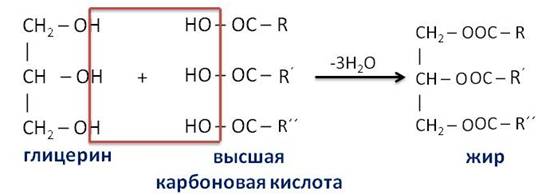
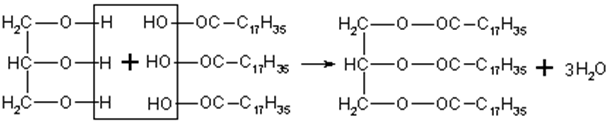
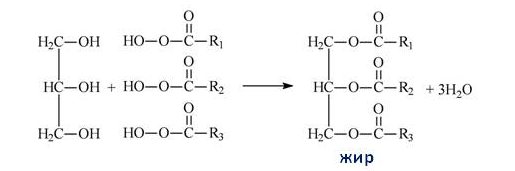
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми (жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.
Химические свойства жиров
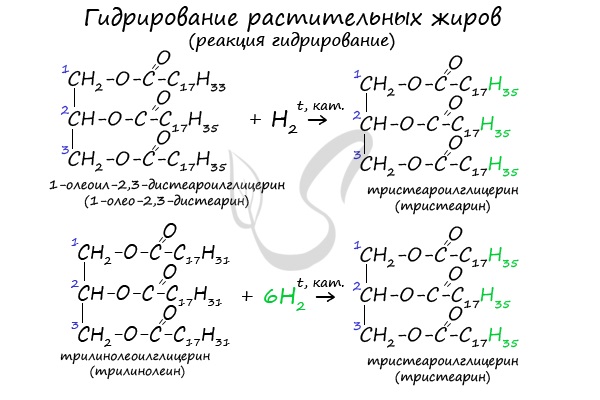
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой промышленности получают маргарин.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Жиры лучше всего растворяются в
При растворимости жидкостей в жидкостях они тем легче смешиваются друг с другом, чем ближе по величине силы взаимодействия молекул в жидкостях. Силу молекулярного взаимодействия приближенно можно охарактеризовать диэлектрической проницаемостью (ε), которая определяет полярность молекул.
Растительные масла – вещества с небольшой полярностью. Для большинства масел диэлектрическая проницаемость при комнатной температуре равна 3,0. 3,2, кроме касторового масла, для которого ε=4,6. 4,7. Этот факт объясняется присутствием большого количества в его триглицеридах остатков рицинолевой кислоты, содержащей полярную гидроксильную группу.
Все растительные масла хорошо растворяются в неполярных гидрофобных растворителях с близкой диэлектрической проницаемостью. К таким растворителям относятся гексан, бензин, бензол, дихлорэтан и некоторые другие.
С ростом разницы значений диэлектрических проницаемостей растворителя и масла их взаимная растворимость ухудшается. Ацетон в этом ряду занимает крайнее положение, его ε = 21,5 (20 о С). Он растворяет масло в любых пропорциях и в то же время смешивается с водой.
Спирты: этиловый, метиловый и изопропиловый ограниченно смешиваются с маслом при комнатной температуре, при нагревании его растворимость повышается. Растворимость масла в спиртах повышается также при увеличении молекулярной массы последних. Это связано с тем, что растворимость жиров в спиртах обусловлена образованием водородных связей гидроксила спиртов с карбоксилом кислот и силами межмолекулярного притяжения между углеводородными радикалами кислот и спиртов.
Растворимость масел в воде ничтожно мала, так как вода является полярной жидкостью (для воды ε = 81).
Обращает на себя внимание растворимость воды в растворителях, так как этот факт имеет практическое значение:
Зависимость между полярностью растворителей и растворимостью в них масла (кроме касторового) и воды представлена в виде схемы (рис.28).
Касторовое масло при комнатной температуре плохо растворяется в бензине, гексане, при нагревании растворимость повышается и может достигнуть полного смешения в любых соотношениях. При комнатной температуре касторовое масло хорошо растворяется в абсолютном этаноле и метаноле.
Рис. 28. Растворимость растительных масел и воды в растворителях разной полярности
В целом, можно отметить следующие группы растворителей:
Природу растворов масел в органических растворителях можно рассматривать как близкую к молекулярной, т.к. абсолютное большинство свойств, которые проявляют мисцеллы, присуще растворам:
Единственным свойством, которое можно отнести к показателям коллоидного состояния, является структурная вязкость. Она обнаружена при вискозиметрических исследованиях растворов некоторых масел в бензоле и ацетоне. Эта структура подвижная, легко разрушается, но отражается на физических свойствах растворов, вызывает отклонение от закона Гагена-Пуазейля о прямолинейной зависимости между давлением и скоростью истечения. Причиной структурной вязкости могут быть вещества, перешедшие при экстракции в раствор вместе с жирами, например, фосфатиды. В этом случае раствор становится дисперсионной средой для коллоидных частиц сопутствующих веществ.
Таким образом, растворы масла в органических растворителях по своим свойствам несколько отличаются от идеальных растворов и не могут в точности подчиняться закону Рауля. Отклонения от данного закона зависят от вида растворителя, температуры, от концентрации мисцеллы и других факторов.
Жиры, их строение и свойства
Урок 37. Химия 9 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Жиры, их строение и свойства»
Жиры, их строение и свойства
Жиры (триглицериды) – это сложные эфиры ттрёхатомного спирта глицерина и высших карбоновых кислот.
Буквой R в уравнении обозначены углеводородные остатки кислоты с большим числом (более пятнадцати) атомов углерода, поэтому их называют высшими карбоновыми кислотами.
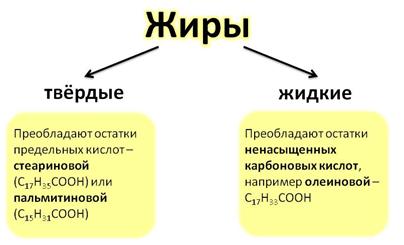
В зависимости от состава кислот различают твёрдые и жидкие жиры. В твёрдых жирах преобладают остатки предельных кислот – стеариновой или пальмитиновой (C17H35COOH, C15H31COOH). А в жидких – преобладают остатки ненасыщенных карбоновых кислот, например олеиновой – C17H33COOH.
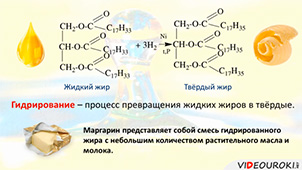
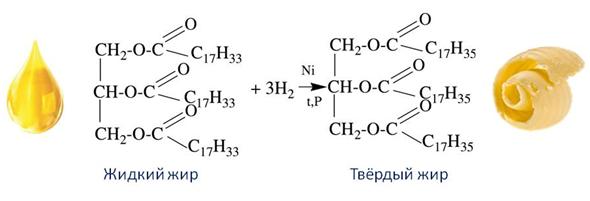
Если остатки непредельных карбоновых кислот присоединят к себе недостающие атомы водорода, то из жидкого жира образуется твёрдый жир. Этот процесс называется гидрированием. Этот процесс широко используют в промышленности – для получения твёрдых жиров. Особо широкое применение имеет маргарин, который представляет собой смесь гидрированного жира с небольшим количеством растительного масла и молока.
Чтобы доказать, что масло содержит остатки ненасыщенных карбоновых кислот, можно провести следующий опыт. Необходимо добавить несколько капель масла в раствор марганцовки и встряхнуть. Происходит обесцвечивание раствора перманганата калия. Эта качественная реакция на кратные связи. Следовательно – масло содержит остатки ненасыщенных карбоновых кислот.
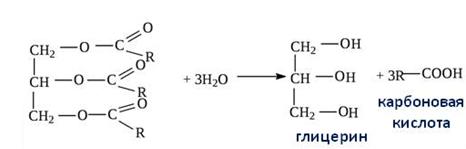
Процесс изучения состава жиров имеет длительную историю. В начале девятнадцатого века француз М.Э. Шеврель доказал, что при гидролизе жиров образуется глицерин и карбоновые кислоты.
В середине девятнадцатого века француз П.Э. Бертло осуществил синтез жира.
По происхождению жиры делят на растительные и животные. Животные жиры – твёрдые вещества. Это, например, говяжий, бараний жир, только рыбий жир является жидким, хотя и является жиром животного происхождения. Растительные жиры – вязкие жидкости, их называют маслами. Это подсолнечное масло, кукурузное, хлопковое, льняное, касторовое. Исключение оставляет кокосовое масло – оно твёрдое.
Жиры легче воды и в ней нерастворимы, но хорошо растворяются в органических растворителях – бензине, хлороформе, четырёххлористом углероде.
Если налить в три пробирки равные объёмы воды, спирта и бензина, а затем в каждую добавить несколько капель масла, а затем встряхнуть, то можно увидеть, что масло не растворяется в воде, в спирте масло немного растворяется, а в бензине полностью растворяется. Если нанести на фильтровальную бумагу несколько капель содержимого второй и третьей пробирки и подождать, пока испариться растворитель, то можно увидеть, что на фильтровальной бумаге образовалось жирное пятно.
Жиры входят в состав животных и растительных организмов и играют большую биологическую роль. Они служат источником энергии для животных и растений. При окислении жиров выделяется в два раза больше энергии, чем при окислении того же количества белков или углеводов. Накапливаясь в подкожных тканях, жиры выполняют и защитную функцию.
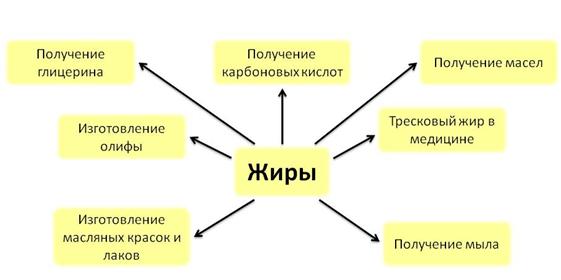
В промышленности из жиров получают глицерин, карбоновые кислоты, масла. Из растительных масел изготавливают олифу, масляные краски, лаки. Богатый витаминами жир тресковой печени используют в медицине.
Из твёрдых жиров получают различные сорта мыла.
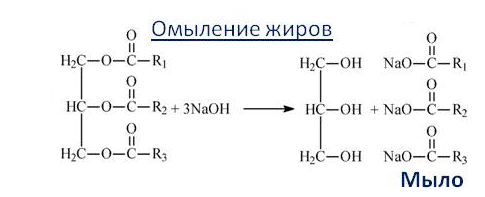
Мыла – это соли жирных кислот.
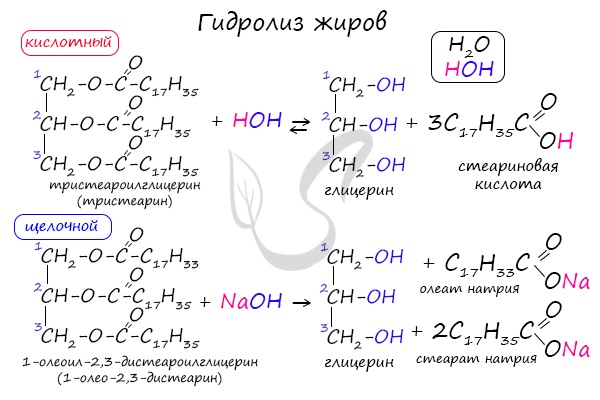
Наиболее распространены натриевые мыла. Натриевое мыло – это твёрдое мыло. Его получают гидролизом жиров раствором едкого натра или соды при нагревании. Этот процесс называют омылением жиров, в результате этого процесса образуется соль органической кислоты и глицерин. Для отделения мыла от глицерина к смеси добавляют водный раствор хлорида натрия, в котором очень плохо растворяется мыло. После чего образуется два слоя: нижний – раствор глицерина и поваренной соли в воде, верхний – получившееся мыло.
Мыла растворяются в воде и обладают моющим действием. В жёсткой воде мыло утрачивает моющее действие. Растворы мыла имеют щелочную среду.
Существует легенда об открытии мыла, согласно которой, когда юноша готовился к празднику, смазал волосы жиром, а затем посыпал голову пеплом, где содержится карбонат калия, а через некоторое время стал смывать пепел, то это вещество начало мылиться.
В качестве моющих средств используют синтетические моющие средства – стиральные порошки. СМС – это натриевые соли сульфокислот или алкилсульфокислот. Растворы СМС имеют нейтральную среду, в жёсткой воде они не утрачивают своих моющих свойств.
Сравним свойства мыла и СМС – порошка. К раствору мыла и СМС добавим несколько капель фенолфталеина. В растворе мыла фенолфталеин стал малинового цвета, потому что раствор мыла имеет щелочную среду, а в щелочной среде фенолфталеин становится малинового цвета, в растворе СМС фенолфталеин не изменил своей окраски, потому что раствор порошка имеет нейтральную среду.
Затем к жёсткой воде в двух пробирках, то есть к воде, содержащей ионы кальция и магния, добавим в первом случае раствор мыла, а во вторую пробирку – раствор порошка и встряхнём. Получается, что в жёсткой воде мыло не пенится, то есть утрачивает свои моющие средства, во второй пробирке пена образовалась, то есть СМС не утрачивает своих моющих свойств в жёсткой воде. Мыло утрачивает свои моющие свойства в жёсткой воде, потому что кальциевые и магниевые соли высших карбоновых кислот нерастворимы и выпадают в осадок.
Таким образом, жиры представляют собой смесь глицерина и высших карбоновых кислот. Для жиров характерны реакции гидролиза. Жидкие жиры при гидрировании превращаются в твёрдые жиры. Жиры являются ценным пищевым энергетическим продуктом, обеспечивающим нормальное функционирование организма человека. К моющим средствам относят мыла и синтетические моющие средства. СМС, в отличие от мыла, сохраняют моющие свойства в жёсткой воде и имеют нейтральную среду.
Форум химиков
Растворители жиров
Растворители жиров
Сообщение PMMA » Чт окт 27, 2011 11:11 am
Re: Растворители жиров
Сообщение amik » Чт окт 27, 2011 11:44 am
Re: Растворители жиров
Сообщение avor » Чт окт 27, 2011 2:00 pm
Re: Растворители жиров
Сообщение amik » Чт окт 27, 2011 3:02 pm
Re: Растворители жиров
Сообщение PMMA » Чт окт 27, 2011 4:00 pm
Re: Растворители жиров
Сообщение amik » Чт окт 27, 2011 4:11 pm
Re: Растворители жиров
Сообщение Любитель_Манниха » Чт окт 27, 2011 7:12 pm
Re: Растворители жиров
Сообщение Tokashi » Пн окт 31, 2011 9:12 am
Re: Растворители жиров
Сообщение Just8 » Ср фев 03, 2016 10:26 am
Ну, естественно, это не должно разъедать резинки и т.пр. в системе охлаждения. Так сказать, не навреди.
Re: Растворители жиров
Сообщение chemist » Ср фев 03, 2016 10:57 am
Соль, лимон, мыло или средство для посуды: чем свести с одежды жирное пятно
Жирные пятна на одежде, которые оставляют макароны, жареная картошка или бургеры, вывести зачастую трудно. Порой кажется, что эти кляксы даже более въедливые, чем пятна на Солнце. Все знают, что смыть их, сполоснув вещь в воде, невозможно. Жир не растворяется в воде. Как же привести одежду в порядок?
Интернет пестрит десятками рецептов, однако любимая футболка может просто не выдержать всех этих испытаний бензином, скипидаром и нашатырем. Программа «НашПотребНадзор» взяла пять футболок и пять средств первой помощи от жирных пятен: соль, мыло, уксус, лимонный сок и средство для мытья посуды.
Чтобы пятно от жареной курицы или картошки не превратилось в постоянный принт, согласно народным лайфхакам, рекомендуется эти средства применять как можно скорее. Профессиональные химики с этим согласны. В составе жирной капли всегда есть вода. И она поначалу мешает жирной кляксе впитаться в ткань, ведь влага стимулирует силы поверхностного натяжения, благодаря которым растет способность молекул капли сохранять целостность. Но этот эффект сохраняется всего пару минут или меньше, потому что ткани волокна материала, имеющего, как правило, ячеистую структуру, начинают впитывать воду из жирной капли, помогая последней быстрее испаряться. С течением времени в эти микроотверстия ткани плотнее проникает и жир. Взаимодействуя с кислородом, он быстро окисляется, темнеет и затвердевает. Именно такие пятна называют въевшимися и трудно выводимыми. Соль, сок лимона, уксус, мыло или средства для мытья посуды, если верить народным советам, мешают жиру крепко сцепиться с тканью в ожидании стирки.
Для эксперимента растекшийся горячий жир от бифштексов быстро засыпаем обычной поваренной солью, которая отлично притягивает влагу и, по идее, должна впитать в себя и воду, и жир быстрее, чем поверхность ткани. Кроме того, соль мешает жиру еще и на молекулярном уровне.
Лимонная кислота, которая содержится в лимоне и во многом обуславливает его кислый вкус, будет растворять жир. Многие уверены, что это поможет вещь отстирать.
Не меньше поклонников и у другой кислоты уксусной. Химики ее эффективность подтверждают. Она хорошо растворяет очень многие органические соединения, в том числе и жиры. Но использовать надо не концентрированную эссенцию, а лишь раствор, чтобы кислота не разъела тонкую ткань футболки.
В Интернете часто советуют для борьбы с жирными пятнами применять средство для мытья посуды. Его задача растворять жир на стенках кастрюль, на тарелках и ложках, поэтому многие уверены, что веществам, входящим в состав моющих средств, все равно, где уничтожать загрязнения на фарфоре или хлопке.
Жир очень сложно смыть водой, поскольку вода с ним почти не взаимодействует, ее молекулы плохо захватывают с собой молекулы жира. Задача поверхностных активных веществ в составе моющих средств прикрепить молекулы жира к молекулам воды. Они образуют частички, внутри которых остается жир, и потом мы все это смываем водой и поверхность остается чистой. вещества есть и в более дешевом хозяйственном мыле, поэтому многие советуют атаковать жирные пятна им. Это натриевая соль различных жирных кислот.